Alergiczna aspergiloza oskrzelowo-płucna – diagnostyka i leczenie
Alergiczna aspergiloza oskrzelowo-płucna jest zbyt rzadko rozpoznawanym schorzeniem – wskazane jest częstsze podejmowanie diagnostyki w tym kierunku, przede wszystkim u chorych na astmę lub mukowiscydozę. Szacuje się, że choroba może dotyczyć nawet 5 mln ludzi na świecie.
Alergiczna aspergiloza oskrzelowo-płucna (allergic bronchopulmonary aspergillosis, ABPA) należy do rzadko rozpoznawanych chorób układu oddechowego. Dotyczy głównie chorych z grupy ryzyka, jednak diagnostyka w kierunku ABPA jest podejmowana rzadko, często na zaawansowanym etapie zmian. Szacuje się, że opóźnienie rozpoznania sięga nawet 10 lat, a u co najmniej 30 proc. chorych nie jest rozpoznana mimo klinicznej manifestacji[1]. Algorytm diagnostyczny opiera się w dużej mierze na dostępnych powszechnie metodach, takich jak całkowite IgE, testy skórne w kierunku Aspergillus fumigatus, badania obrazowe (HRCT).
Aspergiloza
Narażenie na Aspergillus jest powszechne, jednak zachorowania związane z zakażeniem są rzadkie i dotyczą zaledwie kilku gatunków spośród około 250 przedstawicieli kropidlaka – głównie powodują je Aspergillus fumigatus (około 80 proc.), rzadziej Aspergillus terreus, Aspergillus niger, Aspergillus flavus. Zakażenie Aspergillus najczęściej dotyczy osób z obniżoną odpornością. Do zakażenia zazwyczaj dochodzi drogą wziewną poprzez zainhalowanie spor, obecnych w powietrzu zewnętrznym, zwykle podczas kontaktu z resztkami roślinnymi lub w obrębie budynków poprzez nawiewy. Zakażenie Aspergillus może przebiegać w zróżnicowany sposób – zarówno jako postać nieinwazyjna o lekkim przebiegu, ale też w postać ciężka, prowadząca do zgonu chorego.
Postacie kliniczne zakażenia kropidlakiem Aspergillus fumigatus:
- inwazyjna aspergiloza
• postać zatokowo-płucna
• postać uogólniona
• postać narządowa (dotyczy pojedynczego narządu)
- przewlekła martwicza postać aspergilozy (PMPA)
- grzybniak kropidlakowy – aspergilloma
- alergiczna aspergiloza oskrzelowo-płucna (ABPA).
ABPA dotyczy najczęściej chorych na astmę – dane epidemiologiczne wskazują na zróżnicowaną częstość od 1-2 proc.[2, 3, 4] nawet do 12,9 proc.[5] chorych na astmę oskrzelową. Kazuistyczne przypadki dotyczą chorych z rozstrzeniami oskrzeli, pacjentów po przeszczepieniu płuc, w zespole hiper-IgE.
Patomechanizm
W patomechanizmie ABPA dużą rolę odgrywa złożona reakcja z nadwrażliwości, do której dochodzi w wyniku odpowiedzi na kolonizację dróg oddechowych przez Aspergillus fumigatus[6]. Alergeny rozpuszczalne w wodzie przechodzą przez warstwę nabłonka oskrzelowego, następuje pobudzenie limfocytów Th2, produkcja cytokin głównie IL4, IL5. IL4 pobudza powstawanie IgE (skurcz oskrzeli). IL5 stymuluje powstawanie, dojrzewanie i chemotaksję eozynofilów. IL4 i IL5 wydłużają czas przeżycia eozynofilów, następuje uwalnianie z ziarnistości głównego białka zasadowego (MBP), białka kationowego (ECP), peroksydazy (EPO), neurotoksyny (EPX/EDN).
Ponadto grzybnia Aspergillus f. uwalnia toksyczne metabolity takie jak elastaza, alkaliczna elastolityczna proteaza, których oddziaływanie lokalnie prowadzi do destrukcji tkanki płucnej. Miejscowo również oddziałują substancje sprzyjające przeżyciu zarodników: czynnik hamujący opsonizację oraz restriktocyna, pochodna mitogiliny, która hamuje migrację neutrofili i uwalnianie wolnych rodników.
W przebiegu zapalenia dochodzi do aktywacji zarówno odpowiedzi Th1, jak i Th2 zależnej z powstawaniem przeciwciał IgA, IgG i IgE. Procesy zapalne powodują tworzenie nacieków eozynofilowych w płucach z powstawaniem ziarniniaków w oskrzelach głównych. W świetle oskrzeli występuje gęsty śluz w postaci czopów śluzowych lub odlewów, w których stwierdza się obecność eozynofilów oraz strzępek grzybni. Zaleganie śluzu, oddziaływanie enzymów proteolitycznych oraz mykotoksyn doprowadza do powstawania rozstrzenia oskrzeli.
Obraz kliniczny
Obraz kliniczny ABPA jest zróżnicowany, zależnie od stadium zaawansowania choroby oraz nasilenia zmian radiologicznych. Zwykle dotyczy chorych z niekontrolowaną, ciężką astmą oskrzelową, u których obserwowane są nacieki w płucach, mogą im towarzyszyć rozstrzenia oskrzeli.
Diagnostyka w przypadku podejrzenia aspergilozy oskrzelowo-płucnej powinna być podjęta w przypadku chorego z przejściowo występującymi zmianami śródmiąższowymi, którym towarzyszy eozynofilia. Pacjent podczas wywiadu zwykle wymienia kilka objawów: kaszel z odkrztuszaniem lepkiej, czasem brązowawej wydzieliny, duszność, ból opłucnowy, epizody krwioplucia. Zazwyczaj w badaniu przedmiotowym obecne są świsty, mogą wystąpić trzeszczenia, zwykle przejściowo, po napadzie kaszlu. W ciężkim przebiegu występuje gorączka, dreszcze, uczucie zmęczenia, spadek masy ciała. W zaawansowanym stadium stwierdzane są kliniczne i radiologiczne cechy włóknienia płuc oraz palce pałeczkowate.
Diagnostyka ABPA
Podstawowym badaniem o dużym znaczeniu diagnostycznym, a jednocześnie tanim i szybkim, jest test skórny (skin prick test, SPT) z Aspergillus fumigatus. W przypadku wyniku ujemnego należy wykonać test śródskórny. Ujemny wynik testu skórnego i śródskórnego wskazuje na niewielkie prawdopodobieństwo ABPA. Kolejnym pod względem istotności badaniem jest oznaczenie miana całkowitego IgE – punktem odcięcia jest wartość 417 kU/l. Miano IgE jest zmienne w zależności od aktywności procesu – narasta w okresie pojawiania się zmian radiologicznych, towarzyszy temu wzrost eozynofilii – wówczas miana IgE mogą wzrosnąć nawet 10-krotnie. Obserwacje wskazują jednak, że nawet po zakończeniu leczenia wartość całkowitego IgE u chorych z ABPA nie obniża się poniżej poziomu 417 kU/l. Miana swoistego IgE skierowanego przeciwko alergenom Aspergillus fumigatus są podwyższone – zwykle obserwuje się dwukrotnie wyższe miana w porównaniu z chorymi z atopią wobec Aspergillus, u których występuje nieżyt nosa lub astma. Inne badania diagnostyczne to oznaczenie swoistego IgG przeciwko antygenom Aspergillus (dodatnie u ponad 90 proc. chorych z ABPA)[6]. W badaniach diagnostycznych stosuje się m.in. oznaczenie PCR w surowicy (czułość 66,7 proc., swoistość – 98,7 proc.), a ujemny wynik ma wysokie znaczenie wykluczające (98,0 proc.). Inne badanie o wysokiej czułości to oznaczenie galaktomannanu (czułość 78,4 proc., swoistość 87,5 proc.)[7]. Łączne zastosowanie tych badań zwiększa wykrywalność inwazyjnej aspergilozy do 88,2 proc.[7, 8]. U 40 proc. chorych na ABPA występuje podwyższona eozynofilia (>1000 komórek/dl). Ze względu na przewagę innych badań diagnostycznych obecnie rzadko wykonywane są badania plwociny w kierunku obecności kryształków Charkota-Leydena i skupisk eozynofilów, a także strzępek grzybni Aspergillus fumigatus. Diagnostykę pod kątem ABPA przeprowadza się zgodnie z wytycznymi grupy roboczej International Society for Human and Animal Mycology (ISHAM)[5].
W ostatnich latach modyfikowano kryteria diagnostyczne ABPA, jak też klasyfikację radiologiczną. Grupa robocza ISHAM w oparciu o przegląd literatury dokonała krytycznej analizy dostępnych danych, proponując kryteria diagnostyczne, które są powszechnie dostępne i względnie niedrogie. Schemat diagnostyczny uwzględniający klasyfikację w oparciu o dokument grupy roboczej ISHAM przedstawiono na rycinie 1.
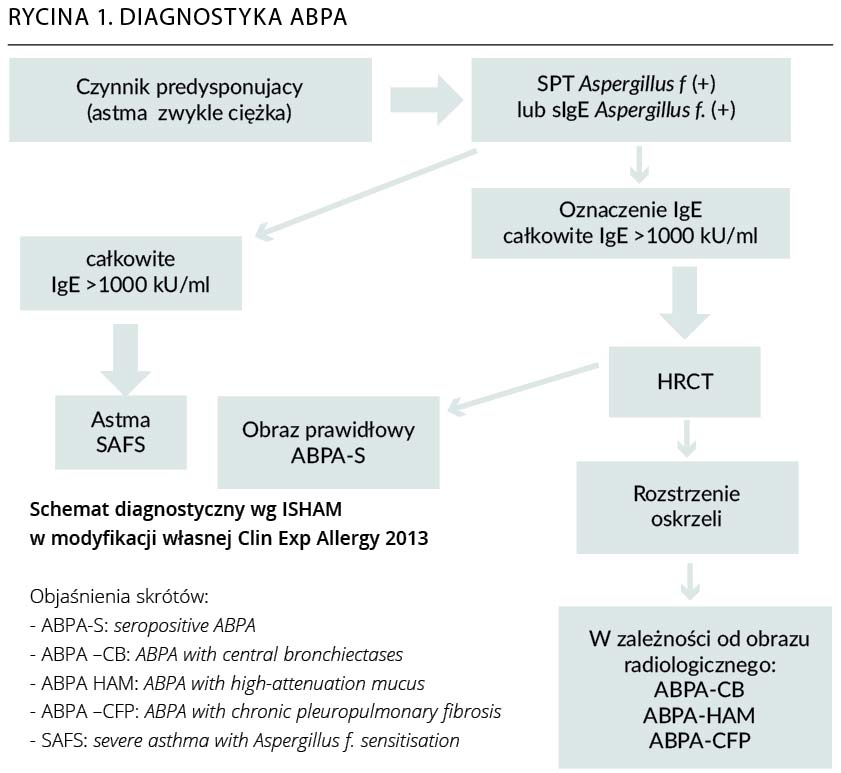
Wcześniej stosowano kryteria według Pattersona i Rosenberga, większość danych publikowanych przed 2013 r. uwzględnia te kryteria. Największe znaczenie dla rozpoznania i oceny zaawansowania mają zmiany radiologiczne.
Minimalne kryteria diagnostyczne dla klasycznej postaci z rozstrzeniami oskrzeli (ABPA-CB) obejmują:
- astma
- rozstrzenie oskrzeli (na wysokości 2/3 wewnętrznego wymiaru klatki piersiowej w obrazie HRCT)
- zmiany miąższowe w radiogramie klatki piersiowej (zwykle górny lub środkowy płat)
- dodatni wynik testu skórnego z Aspergillus fumigatus lub grupy Aspergillus
- całkowite stężenie IgE powyżej 417 kU/l
- podwyższone stężenie IgE i/lub IgG przeciwko Aspergillus fumigatus.
Alergiczna aspergiloza oskrzelowo-płucna bez rozstrzeni oskrzeli (seropozytywna ABPA):
- astma
- zmiany miąższowe w RTG klatki piersiowej (zwykle górny lub środkowy płat) – zmiany mogą być nieobecne
- dodatni wynik testu skórnego z Aspergillus fumigatus lub grupy Aspergillus
- całkowite stężenie IgE powyżej 417 kU/l
- podwyższone stężenie IgE oraz IgG przeciwko Aspergillus fumigatus.
Leczenie
W leczeniu podstawowe znaczenie ma przeciwzapalne działanie leków[8, 9], zwłaszcza wobec znanych z patomechanizmu ABPA zjawisk nadwrażliwości. Dlatego też nadal kluczową rolę odgrywają glikokortykosterydy systemowe (sGKS). Aktualnie zaleca się algorytm w oparciu o sGKS, itrakonazol lub leki te w połączeniu. Itrakonazol jest zalecany w przypadku nawracających zaostrzeń i sterydozależnej astmy[9].
Proponowane algorytmy terapeutyczne:
- schemat z niską dawką sGKS (prednizon 0,5 mg kg/kg/d 2 tygodnie, potem co drugi dzień 6-8 tygodni, następnie redukcja dawki o 5-10 mg co 2 tygodnie, odstawienie leku)
- schemat z wysoką dawką sGKS (prednizon 0,75 mg kg/kg/d 6 tygodni, potem 0,5 mg 6 tygodni, następnie redukcja dawki o 5 mg co 6 tygodni, odstawienie leku)
- schemat z itrakonazolem (200 mg 2 x dziennie z monitorowaniem stężenia leku co 16 tygodni, kursy 4-6 miesięcy lub terapia przewlekła)
- schemat łączony (itrakonazol +sGKS).
Podjęto próby leczenia omalizumabem, trwają badania nad innymi lekami w terapii ABPA. W monitorowaniu efektywności terapii oprócz badań radiologicznych należy dokonywać oceny miana całkowitego IgE (spadek o przynajmniej 25 proc. wartości wyjściowej wskazuje na efektywność terapii), oznaczenie swoistego IgE wobec Aspergillus f. nie ma znaczenia w monitorowaniu leczenia[10].
Podsumowanie
Alergiczna aspergiloza oskrzelowo-płucna jest zbyt rzadko rozpoznawanym schorzeniem – wskazane jest częstsze podejmowanie diagnostyki w tym kierunku, przede wszystkim u chorych na astmę lub mukowiscydozę.
Szacuje się, że ABPA może dotyczyć nawet 5 mln chorych na świecie[9], jednak ze względu na niedorozpoznanie i opóźnienie rozpoznania, częściej dotyczy chorych z długotrwałym przebiegiem, w zaawansowanym stadium choroby. Dlatego aktualne stanowisko grupy roboczej ISHAM[6] wskazuje na potrzebę podjęcia diagnostyki u wszystkich chorych na astmę. Wcześniejsze rozpoznanie może przyczynić się do większej skuteczności terapii ABPA i ograniczyć występowanie powikłań.
Aktualne kryteria ABPA zgodnie z wytycznymi grupy roboczej ISHAM[5]
Kryteria konieczne (muszą być oba obecne):
- dodatni wynik testów skórnych wobec Aspergillus fumigatus lub zwiększone stężenie IgE przeciwko Aspergillus fumigatus
- zwiększone stężenie całkowitego IgE (zwykle ponad 1000IU/ml – jeśli chory spełnia wszystkie inne kryteria dopuszczalne jest stężenie niższe)
Inne kryteria (minimum dwa muszą być obecne):
- obecność precypityn w kierunku A. fumigatus lub zwiększone stężenie w osoczu swoistych IgG w kierunku Aspergillus
- zmiany radiologiczne charakterystyczne dla ABPA (zmiany przejściowe lub utrwalone)
- eozynofilia >500 u chorych nieleczonych GKS
Czynniki predysponujące (minimum jedno obecne):
- astma
- mukowiscydoza
tekst: dr n. med., dr n. hum. Małgorzata Farnik, adiunkt, Katedra i Klinika Pneumonologii ŚUM,
kierownik prof. dr hab. n. med. Adam Barczyk
Piśmiennictwo:
1. A. Chakrabarti, S. Sethi, D.S. Raman, D. Begera, Eight-year study of allergic bronchopulmonary aspergillosis in an Indian teaching hospital, Mycoses, 2002; 45: 295-9.
2. P.A. Greenberger, Allergic bronchopulmonary aspergillosis, J Allergy Clin Immunol 2002, 110-685-692.
3. P.A. Greenberger, Clinical aspects of allergic aspergillosis, Front Biosci. 2003; 8: 119-127.
4. B. Mahde, P.A. Greenberger, Allergic bronchopulmonary aspergillosis, Allergy Asthma Proc 2004; 25: S38-S39.
5. R. Agarwal, A. Chakrabarti, A. Shah, D. Gupta, J.F. Meis, R. Guleria, R. Moss, D.W. Denning, Allergic bronchopulmonary asperillosis: review of literature and proposal of new diagnostic and classification criteria, Clin Exp Allergy 43: 850-873.
6. R. Agarwal, A.N. Aggarwal, D. Gupta, Prevelance of Aspergillus hypersensitivity in patients with bronchial asthma: a systemic review, Int J Tuberc Lung Dis 2009. 34: 23-32.
7. S. Imbert, L. Gauthier, I. Joly, J.Y. Brossas, M. Uzunov, F. Touafek, S. Brun, D. Mazier, A. Datry, F. Gay, A. Fekkar, Aspergillus PCR in serum for the diagnosis, follow-up and prognosis of invasive aspergillosis in neutropenic and non-neutropenic patients, Clin Microbiol Infect. 2016 Feb 16. pii: S1198-743X(16)00109-9. doi: 10.1016/j.cmi.2016.01.027. [Epub ahead of print].
8. J. Cadena, G.R. 3rd Thompson, T.F. Patterson, Invasive Aspergillosis: Current Strategies for Diagnosis and Management, Infect Dis Clin North Am. 2016 Mar;30(1):125-42. doi: 10.1016/j.idc.2015.10.015.
9. L. Leonardi, B.L. Cinicola, R. Laitano, M. Duse, Allergic Bronchopulmonary Aspergillosis: Diagnostic and Treatment Challenges, J Pulmon Respir Med, 2016; 6:4.
10. R. Agarwal, I. Sehgal, S. Dhooria, A. Aggarwal, Developments in the diagnosis and treatment of allergic bronchopulmonary aspergillosis, 2016.
11. R. Agarwal, A. Aggarwal, I.S. Sehgal, S. Dhooria, D. Behera, A. Chakrabarti, Utility of IgE (total and Aspergillus fumigatus specific) in monitoring for response and exacerbations in allergic bronchopulmonary aspergillosis, Mycosis 2016, Jan 59 (1).

 Instytut Nagrody Zaufania Złoty OTIS
Instytut Nagrody Zaufania Złoty OTIS